 |
国家兽药产业技术创新联盟 National veterinary drug industry technology innovation alliance |
用户登录
联系我们
|
服务创造价值、存在造就未来
近日,中国农业科学院兰州兽医研究所/兰州大学动物医学与生物安全学院王帅教授团队在肝病与肠道免疫交叉领域取得突破性进展。该研究首次系统阐明了肝包虫病及肝硬化等其他肝脏疾病中胆汁酸代谢紊乱导致"口腔-肠道屏障"崩溃的分子机制,为肝源性肠炎的防治提供了全新干预策略,相关成果已发表于Cell旗下期刊《Cell Reports》上。
包虫病是一种严重的人兽共患寄生虫病,具有肝脏寄生嗜性,可导致肝硬化甚至肝衰竭。当前对于肝包虫引起的病理损伤及其对宿主健康影响,研究尚较少。长期以来,本项目研究团队以及其他研究团队均发现,肝包虫病及其他肝脏疾病(如肝硬化、肝癌、非酒精性脂肪肝病和酒精性肝病)患者常伴随肠道菌群失衡和肠炎症状。由于机制不明,此类肠炎缺乏针对性治疗手段。
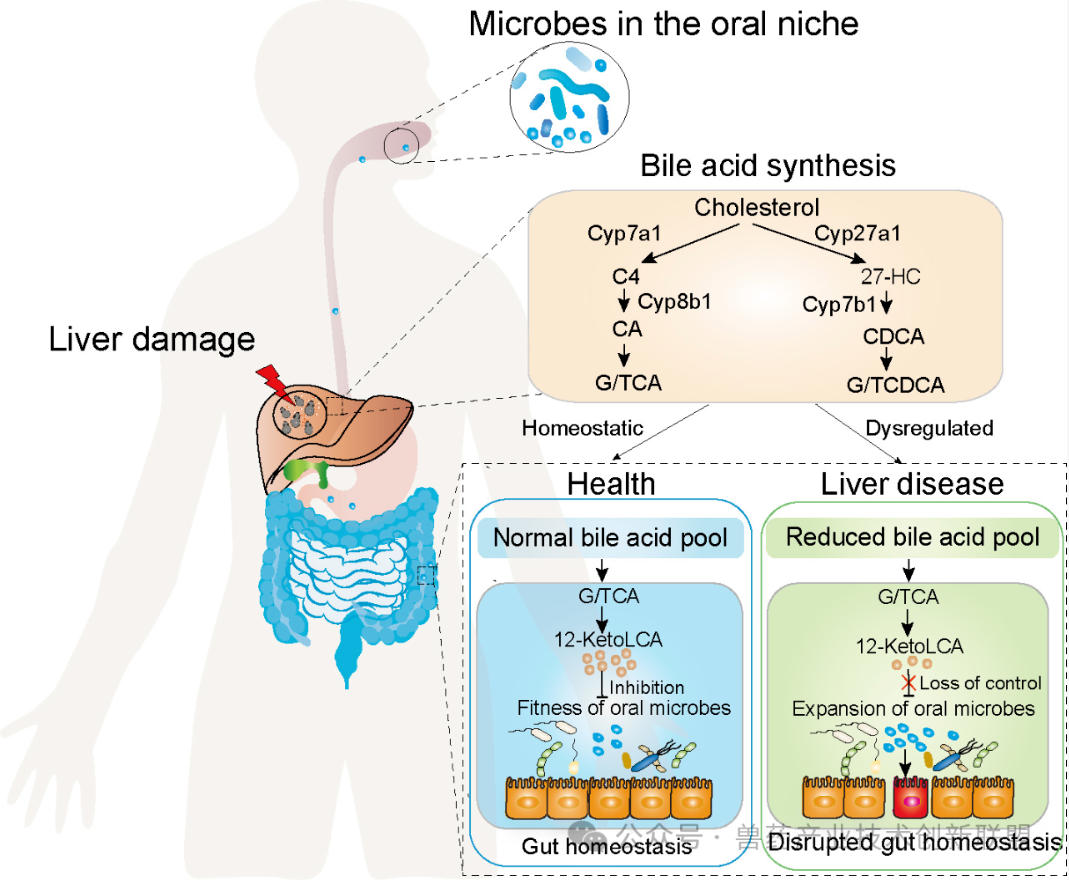
研究团队利用近4年时间,整合临床队列分析(涵盖泡型包虫病、囊型包虫病及肝硬化、非酒精性脂肪性肝病(NAFLD等肝病)、多组学技术、机器学习、基因治疗以及系统的动物模型实验,揭示了肝脏疾病跨器官调控的共性病理机制。口腔菌“入侵”肠道:包虫病及肝硬化等疾病发生后肠道中口腔来源的链球菌显著富集,这些菌群异位定植直接驱动肠道炎症;胆汁酸“护盾”失效:机制上,肝脏损伤导致胆汁酸稳态失衡,关键活性分子次级胆汁酸12-酮石胆酸(12-KetoLCA)水平骤降。该分子为肠道菌群以初级胆汁酸代谢产生,可通过破坏微生物细胞膜和引起跨膜物质转运紊乱,强效抑制口腔来源促炎菌群,其缺失使肠道丧失"化学屏障"功能;调控通路提供关键“靶点”:内质网以及线粒体细胞色素P450酶(如Cyp7a1和Cyp8b1)通路介导的胆汁酸代谢紊乱是核心调控节点,通过腺相关病毒AAV载体基因治疗方案修复该通路或直接补充12-KetoLCA均可恢复肠道屏障,有效治疗口腔菌群驱动的肠炎。
本项目是寄生虫学与肠道微生态学的交叉研究成果,系统阐明了口腔菌群转移和肠道免疫稳态失衡的关键机制,具有普适性意义,为肝源性肠炎提供全新治疗靶点。该研究得到了国家重点研发计划项目(2022YFD1800200)以及中国农业科学院农业创新工程计划的资助。王帅研究员和郭爱疆研究员为本论文通讯作者,王玉桂博士、牟文杰博士、管健硕士为论文的共同第一作者。文章链接:Bile acid synthesis dysregulation in liver diseases promotes ectopic expansion of oral streptococci in the intestine: Cell Reports
王帅教授团队,围绕肠道寄生虫、肠道微生态与宿主免疫互作机理领域,近期取得系列研究成果,已在Nature Communications、Cell Reports、Nature Aging、The ISME Journal、Gut Microbes、Microbiome、eBiomedicine、npj Biofilms and Microbiomes、mBio等知名期刊发表论文30余篇,获得F1000prime优秀论文、ESI高被引论文、MIT技术评论等推荐,促进了寄生虫病感染防治以及宿主免疫相关疾病治疗手段开发。
国家兽药产业技术创新联盟 National veterinary drug industry technology innovation alliance |
扫一扫  |
| 联系电话:010-62103991转611 联系地址:北京市海淀区中关村南大街8号 备案:京ICP备20024024号 |